各位同學在查看時請點擊全屏查看
2018年銅仁中考化學復習題
(時間:90分鐘 滿分:100分)
可能用到的相對原子質量:H 1 C 12 O 16 Na 23 Cl 35.5 K 39
一、選擇題(每小題只有一個選項符合題意,每小題3分,共45分)
1.下列過程中,只發生物理變化的是( )
A.銅器銹蝕????????????? B.酒精揮發
C.海水制堿????????????? D.牛奶變酸
解析:酒精揮發的過程中沒有新物質生成,屬于物理變化。
答案:B
2.下圖是某化學反應的示意圖(“![]() ”與“
”與“![]() ”分別代表不同元素原子),該反應可能為( )
”分別代表不同元素原子),該反應可能為( )
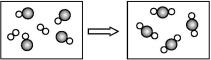
A.氫氣的燃燒
B.水的電解
C.甲烷的燃燒
D.一氧化碳的燃燒
解析:從圖中看出,反應物是一種單質和一種化合物,且每個化合物的分子是由兩個不同種類的原子構成,生成物是一種化合物,故只有D符合題意。
答案:D
3.下面是某同學對部分化學知識的歸納,其中不正確的一組是( )
A.化學與健康 | B.實驗記錄 |
①人體缺鐵會引起貧血 ②糖類是人體能量的主要來源 ③用活性炭凈水器可凈化飲用水 | ①用10 mL量筒量取7.5 mL水 ②用pH試紙測得蘋果汁的pH為3 ③用托盤天平稱取5.6 g鐵粉 |
C.化學與能源 | D. |
①化石燃料是可以再生的能源 ②可以開發的能源有太陽能、風能等 ③氫能是污染小、能量高的理想能源 | ①廚房煤氣管漏氣應關閉閥門并開窗通風 ②實驗時碰倒酒精燈引起著火用濕布蓋滅 ③冬天用煤爐取暖應保證室內通風 |
解析:化石燃料是不可再生能源,故C錯誤。
答案:C
4.如圖是“用雙氧水制取一瓶氧氣”實驗的主要步驟,其中操作錯誤的是( )
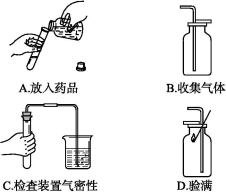
解析:A.向試管中傾倒液體藥品時,瓶塞要倒放,標簽要對準手心,瓶口緊挨,圖中所示操作正確;B.氧氣密度比空氣的大,可用向上排空氣法收集,圖中所示操作正確;C.檢查裝置氣密性的方法:把導管的一端浸沒在水里,用手緊握容器外壁,若導管口有氣泡冒出,松開手后,導管中形成一段穩定的水柱,則裝置不漏氣,圖中所示操作正確;D.檢驗氧氣是否收集滿時,應將帶火星的木條放在集氣瓶口,不能伸入瓶中,圖中所示操作錯誤。
答案:D
5.下列說法錯誤的是( )
A.在鋼鐵表面涂油漆可以防止鐵生銹
B.10 mL酒精和10 mL水混合后體積小于20 mL,是因為分子變小了
C.撲滅森林火災時,可開挖防火隔離帶![]() ,其目的是隔絕可燃物
,其目的是隔絕可燃物
D.用鉛銻合金制作保險絲,是因為熔點低
解析:10 mL酒精和10 mL水混合后體積小于20 mL,是因為分子間的間隔變小了,而分子的大小沒有變化,故B錯誤。
答案:B
6.對于反應:X+2NaOH![]() 2Y+Cu(OH)2↓,下列分析中正確的是( )
2Y+Cu(OH)2↓,下列分析中正確的是( )
A.Y一定是氯化鈉
B.X和Y的相對分子質量之差為18
C.X可能是CuCl2或Cu(NO3)2[來源:.Com]
D.Y可能是Na2SO4
解析:由X+2N![]() aOH
aOH![]() 2Y+Cu(OH)2↓可知,該反應是堿與鹽發生的復分解反應,由反應可知Y是一種鈉鹽,可以是氯化鈉或硝酸鈉,A項錯誤;設X的相對分子質量為m,Y的相對分子質量為n,依據質量守恒定律,反應前后各物質的相對分子質量之和相等可知,m+80=2n+98,m-2n
2Y+Cu(OH)2↓可知,該反應是堿與鹽發生的復分解反應,由反應可知Y是一種鈉鹽,可以是氯化鈉或硝酸鈉,A項錯誤;設X的相對分子質量為m,Y的相對分子質量為n,依據質量守恒定律,反應前后各物質的相對分子質量之和相等可知,m+80=2n+98,m-2n![]() =18,B項錯誤;若X是CuCl2或Cu(NO3)2則符合題意,C項正確;根據題意可知Y中含有一個鈉離子和一個酸根離子,故Y不是硫酸鈉,D項錯誤。
=18,B項錯誤;若X是CuCl2或Cu(NO3)2則符合題意,C項正確;根據題意可知Y中含有一個鈉離子和一個酸根離子,故Y不是硫酸鈉,D項錯誤。
答案:C
7.下列實驗操作不正確的是( )
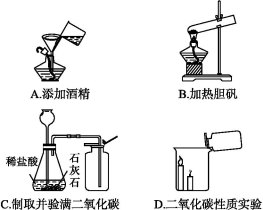
解析:給試管里的固體加熱時,試管口應略向下傾斜,以防試管炸裂,B項錯誤。
答案:B
8.依據國家相關法律規定,機動車駕駛員醉駕將受到刑事處罰。檢測駕駛員是否酒后駕車,可用一種裝有重鉻酸鉀(K2Cr2O7)的儀器。在K2Cr2O7中Cr元素的化合價是????????????? ( ![]() )
)
A.+2價
B.+3價
C.+6價
D.+7價
解析:鉀元素顯+1價,氧元素顯-2價,設鉻元素的化合價是x,根據在化合物中正負化合價代數和為零,可得:(+1)×2+2x+(-2)×7=0,則x=+6價。
答案:C
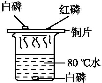
9.用如圖所示裝置探究燃燒的條件,已知白磷的著火點低于80 ℃,紅磷的著火點高于200 ℃。有關該實驗的說法正確的是( )
A.該實驗只能得出燃燒需要氧氣這一結論
B.該實驗說明燃燒需要達到可燃物的著火點
C.該實驗現象是銅片上的白磷不燃燒,紅磷燃燒
D.該實驗使用了相同的可燃物
解析:紅磷和白磷是兩種不同的物質,著火點不同,銅片上的紅磷不燃燒白磷燃燒是因為溫度沒有達到紅磷的著火點;水下白磷不燃燒是因為缺少氧氣,該實驗說明了燃燒除![]() 了需要
了需要![]() 可燃物外,可燃物還必須接觸氧氣,同時溫度必須達到可燃物的著火點。
可燃物外,可燃物還必須接觸氧氣,同時溫度必須達到可燃物的著火點。
答案:B
10.某學生為了驗證鐵、鋅、銅三種金屬的活動性順序,設計了四種方案:①將Zn、C![]() u分別加入到FeSO4溶液中;②將Fe、Cu分別加入到ZnSO4溶液中;③將Zn分別加入到FeSO4、CuSO4溶液中;④將Fe分別加入到ZnSO4、CuSO4溶液中。其中可行的是( )
u分別加入到FeSO4溶液中;②將Fe、Cu分別加入到ZnSO4溶液中;③將Zn分別加入到FeSO4、CuSO4溶液中;④將Fe分別加入到ZnSO4、CuSO4溶液中。其中可行的是( )
A.①④????????????? B.①②
C.②③????????????? D.③④
解析:①將Zn、Cu分別加入到FeSO4溶液中,鋅能與硫酸亞鐵反應,說明金屬活動性順序鋅在鐵的前面,銅不與![]() 硫酸亞鐵反應,說明金屬活動性順序銅在鐵的后面,可以驗證鐵、鋅、銅三種金屬的活動性順序;②將Fe、Cu分別加入到ZnSO4溶液中,都不反應,說明金屬活動性順序鐵和銅都在鋅的后面,但是不能證明鐵和銅的順序;③將Zn分別加入到FeSO4、CuSO4溶液中,鋅能與硫酸亞鐵和硫酸銅反應,說明金屬活動性順序鋅在鐵和銅的前面,不能證明鐵和銅的順序;④將Fe分別加入到ZnSO4、CuSO4溶液中,鐵與硫酸鋅不反應,說明金屬活動性順序鐵在鋅的后面,鐵能與硫酸銅反應,說明金屬活動性順序鐵在銅的前面,能驗證鐵、鋅、銅三種金屬的活動性順序。[來源:Z*xx*k.Com]
硫酸亞鐵反應,說明金屬活動性順序銅在鐵的后面,可以驗證鐵、鋅、銅三種金屬的活動性順序;②將Fe、Cu分別加入到ZnSO4溶液中,都不反應,說明金屬活動性順序鐵和銅都在鋅的后面,但是不能證明鐵和銅的順序;③將Zn分別加入到FeSO4、CuSO4溶液中,鋅能與硫酸亞鐵和硫酸銅反應,說明金屬活動性順序鋅在鐵和銅的前面,不能證明鐵和銅的順序;④將Fe分別加入到ZnSO4、CuSO4溶液中,鐵與硫酸鋅不反應,說明金屬活動性順序鐵在鋅的后面,鐵能與硫酸銅反應,說明金屬活動性順序鐵在銅的前面,能驗證鐵、鋅、銅三種金屬的活動性順序。[來源:Z*xx*k.Com]
答案:A
11.金剛石、石墨和C60的化學性質相似,物理性質卻有很大的差異,其原因是( )
A.金剛石、石墨和C60里碳原子的排列方式不同
B.構成它們的原子數目不同
C.金剛石、石墨和C60由不同種原子構成
D.構成它們的原子大小不同
解析:因為金剛石、石墨、C60中碳原子的排列方式不同,導致三者物理性質有很大差異。
答案:A

12.元素周期表是學習和研究化學的重要工具。右表是元素周期表的一部分,A~F代表六種不同短周期元素。下列說法不正確的是( )
A.原子序數E<C
B.A、D同族
C.A、B同周期
D.C、F化學性質相似
解析:在元素周期表中,同一橫行表示同一周期,同一周期具有相同的電子層數;同一縱行表示同一族,同一族最外層具有相同的電子數,且從上到下電子層數依次增加。E與F在同一周期,C與F屬于同一族,F比C多一個電子層,因此E比C多一個電子層,故原子序數E>C,故A錯誤。
答案:A
13.用石灰水、銅片、鹽酸、碳酸鈉、石灰石五種物質進行下列實驗,其中無法完成的是( )
A.制氫氧化鈉
B.制硫酸銅
C.制二氧化碳
D.制氯化鈉
答案:B
14.低鈉鹽是將普通碘鹽中的部分氯化鈉用氯化鉀代替,有調節體內Na+、K+平衡及預防高血壓的功能。下圖為某低鈉鹽的相關說明,如果一個人每天攝入食鹽的質量為6 g,則食用低鈉鹽比普通碘鹽每天少攝入鈉元素的質量是( )
品名:加碘低鈉鹽
凈重:400 g
成分含量:
NaCl:70%
KCl:29%
碘酸鉀(KIO3)![]() :(以I計算)40 mg/kg
:(以I計算)40 mg/kg
其他:不含K+、Na+
A.0.68 g????????????? B.45.6 g
C.0.71 g????????????? D.1.8 g
解析:由標簽信息可求出食用低鈉鹽比普通碘鹽每天少吃鈉元素質量:6 g×![]() ×100%-6 g×70%×
×100%-6 g×70%×![]() ×100%≈0.71 g。
×100%≈0.71 g。
答案:C
15.下列所示圖像能正確反映對應的實驗或事實的是( )
| A | B | C | D |
圖像 |
|
|
|
|
實驗或事實 | 向pH=12的Ca(OH)2溶液中不斷加水稀釋 | 20 ℃時,向一杯不飽和的KNO3溶液中逐步加入KNO3晶體 | 向稀鹽酸中滴加過量的燒堿溶液 | 將一定質量的碳在密閉容器中(含空氣)加熱 |
解析:向Ca(OH)2溶液中加水稀釋,溶液仍顯堿性,pH不會等于或小于7;20 ℃時,向不飽和KNO3溶液中逐步加入KNO3晶體,開始KNO3晶體溶解,溶質質量分數增大,當溶液達到飽和時,KNO3![]() 晶體不再溶解,溶質質量分數不變;向稀鹽酸中滴加過量的燒堿溶液,開始溶液pH<7,當燒堿過量,溶液pH>7,圖像起點pH<7,終點pH>7,故A、B、C均不正確。根據質量守恒定律可知,反應前后密閉容器內物質的總質量不變,故D正確。
晶體不再溶解,溶質質量分數不變;向稀鹽酸中滴加過量的燒堿溶液,開始溶液pH<7,當燒堿過量,溶液pH>7,圖像起點pH<7,終點pH>7,故A、B、C均不正確。根據質量守恒定律可知,反應前后密閉容器內物質的總質量不變,故D正確。
答案:D
二、填空題(本題包括5個小題,共23分)
16.(4分)根據所學知識,完成下列填空。
(1)米飯富含的營養物質主要是 。
(2)陶瓷、不銹鋼、金剛石、石墨四種物質中,屬于金屬材料的是 。
(3)“沙里淘金”說明黃金在自然界中能夠以 (填“單質”或“化合物”)形式存在。
(4)通常所說的煤氣中毒是指由 (填化學式)引起的中毒。
解析:(1)米飯中富含淀粉,淀粉屬于糖類;(2)金屬材料包括純金屬和合金,不銹鋼屬于合金;(3)由于金的化學性質非常穩定,在自然界中主要是以單質形式存在;(4)煤氣中毒實際上是一氧化碳中毒,是一氧化碳與血紅蛋白結合,使氧喪失了與血紅蛋白結合的機會,導致人體缺氧。
答案:(1)糖類
(2)不銹鋼
(3)單質
(4)CO
17.(4分)(1)某地河水中水生植物大面積爆發,水草瘋長,魚蝦幾乎絕跡,產生該現象的主要原因是河水中 兩種元素含量過高。
(2)汽車尾氣是產生空氣污染的因素之一。
①汽車使用的汽油、柴油是把熱的原油按照各成分 的不同進行分離得到的。汽油的主要成分是碳氫化合物,請你推測汽車尾氣中氮元素的主要來源是 。
②某汽車采用的稀薄燃燒發動機具有高效、經濟、環保的優點。普通汽車發動機中汽油與空氣的質量比為1∶15,稀薄燃燒發動機中汽油與空氣的質量比可達1∶25,與普通發動機相比,稀薄燃燒發動機可以促進燃料的燃燒,請你從微觀上加以解釋 。
稀薄燃燒發動機對于節能減排的意義在于 。
(3)“低碳生活從我做起”,請你從氧循環的角度說明生活中紙張雙面使用的意義 。
解析:(1)水體中N、P含量過高,會導致水體富營養化,使水生植物瘋長,造成水體缺氧,使水質惡化。(2)①用原油制取汽油、柴油等產品是利用蒸餾(或分餾)的方法,其主要原理就是依據原油中各種成分沸點的不同進行分離;依據質量守恒定律,化學反應前后元素的種類不變,汽油中不含氮元素,汽油在燃燒過程中遇到空氣,所以推測氮元素的主要來源應該是空氣中的氮氣。②增大反應物的濃度和反應物的接觸面積,可以使燃料燃燒更加充分。稀薄燃燒發動機與普通汽車發動機相比,單位體積內氧分子的數目較多,與燃料分子碰撞的幾率大,使燃料燃燒更加充分;稀薄燃燒發動機中燃料燃燒更加充分,提高了燃料的利用率,減少了因燃料燃燒不充分而產生的一氧化碳和碳顆粒的排放。
答案:(1)N、P
(2)①沸點 空氣 ②稀薄空氣發動機中單位體積內氧分子的數目較多,與燃料分子碰撞的幾率大 提高了燃料的利用率,減少了CO和碳顆粒的排放
(3)可以減少森林的砍伐,從而有效地保護綠色植物,使空氣中氧氣的含量保持相對穩定
18.(5分)化學是研究物質的,而物質是由肉眼看不到的分子、原子或離子等微觀粒子構成的,讓我們從五彩繽紛的宏觀世界步入充滿神奇色彩的微觀世界。
(1)金秋十月,丹桂飄香,從分子的角度分析其原因是 。
(2)下圖是某化學反應的微觀示意圖,依據此圖回答下列問題:
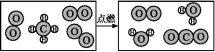
反應物中化合物的化學式為 ,生成物中各物質的粒子個數比是 ,從微觀的角度還能獲得一條關于物質變化的信息是 。
(3)下圖是兩種溶液恰好完全反應的微觀示意圖,此反應的化學方程式為 ,
反應后所得溶液中含有的粒子有 (填符號)。
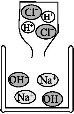
解析:(1)能聞到丹桂飄香是由于分子不斷運動。(2)由微觀示意圖可知,反應物為O2和CH4,化合物為CH4,生成物為H2O和CO2,其個數比為2∶1,在化學變化中,反應前后原子的種類、數目、質量都不變等。(3)由微觀示意圖可知反應物為HCl和NaOH,生成NaCl和H2O,恰好反應后所得溶液為NaCl溶液,粒子有Na+、Cl-和H2O。
答案:(1)分子不斷運動
(2)CH4 2∶1或1∶2 在化學反應中,反應前后原子種類、數目保持不變,原子的質量沒有改變
(3)HCl+NaOH![]() NaCl+H2O H2O、Na+、Cl-
NaCl+H2O H2O、Na+、Cl-
19.(6分)水是我們寶貴的資源,請回答關于水的問題。

(1)凈水器中經常使用活性炭,主要利用活性炭的 性。
(2)要證明某水樣是硬水還是軟水,可向其中加入 。
(3)通過如圖實驗我們認識了水是由氫元素和氧元素組成的,此反應中沒有改變的微粒是 (填名稱),試管“1”中的氣體是 。
(4)水是常見溶劑,現將200 g 30%的氫氧化鈉溶液稀釋為10%,需加水 mL(水的密度為1 g·mL-1),若用量筒量取水時俯視讀數,所得氫氧化鈉溶液的溶質質量分數 (填“大于”或“小于”)10%。
解析:(1)由于活性炭具有吸附性,在凈水器中經常使用活性炭來吸附異味和色素;(2)要證明某水樣是硬水還是軟水,可向其中加入肥皂水,產生浮渣多的是硬水;(3)在化學變化中分子分成原子,原子重新組合形成新物質的分子,因此在電解水的實驗中沒有改變的微粒是氫原子和氧原子,試管“1”中的氣體是氫氣;(4)溶液稀釋過程中溶質質量不變,設需加水的質量是x,則200 g×30%=(200 g+x)×10%,解得:x=400 g,即需加水的體積是400 mL,若用量筒量取水時俯視讀數,所量取的水偏少,所得氫氧化鈉溶液的溶質質量分數大于10%。
答案:(1)吸附
(2)肥皂水
(3)氫原子和氧原子 氫氣
(4)400 大于
20.(4分)實驗室有一包含有少量MgCl2和CaCl2的粗鹽,某小組同學要得到純凈的氯化鈉固體,進行了如下實驗。請回答相關問題:
第一步 除去氯化鎂
將粗鹽加水溶解,向其中加入過量的氫氧化鈉溶液并攪拌,產生白色沉淀,過濾。發生反應的化學方程式為 。
某同學提出:“如果把氫氧化鈉溶液換成氫氧化鉀溶液,行不行?”小組同學經討論,一致認為不可行。理由是 。
第二步 除去氯化鈣
向濾液中加入過量的 溶液并攪拌![]() ,產生白色沉淀,過濾。
,產生白色沉淀,過濾。
第三步 得到氯化鈉固體
向第二步實驗后的濾液中加入過量的稀鹽酸并攪拌,加熱蒸發,得到氯化鈉固體。加入過量稀鹽酸的目的是 。
解析:第一步中如果用KOH溶液,則2KOH+MgCl2![]() Mg(OH)2↓+2KCl,會引入KCl雜質;第二步中的反應:CaCl2+Na2CO3
Mg(OH)2↓+2KCl,會引入KCl雜質;第二步中的反應:CaCl2+Na2CO3![]() CaCO3↓+2NaCl;第三步中由于前兩步加入的是過量的NaOH、Na2CO3,故應加入過量稀鹽酸。
CaCO3↓+2NaCl;第三步中由于前兩步加入的是過量的NaOH、Na2CO3,故應加入過量稀鹽酸。
答案:MgCl2+2NaOH![]() Mg(OH)2↓+2NaCl
Mg(OH)2↓+2NaCl
引入氯化鉀(或引進新雜質)
碳酸鈉(或Na2CO3)
除去過量的氫氧化鈉和碳酸鈉
三、簡答題(本題包括2個小題,共10分)
21.(3分)小明同學繪制了如圖所示A、B兩種固體物質的溶解度曲線:
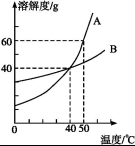
(1)當溫度為 ℃時,A物質與B物質的溶解度相等。
(2)若將B物質從溶液中結晶析出,宜采用的方法是 。
(3)我國有許多鹽堿湖,湖中溶有大量的NaCl和Na2CO3,那里的人們“冬天撈堿,夏天曬鹽”。據此你認為圖中 (填“A”或“B”)物質的溶解度曲線與純堿的相似。
解析:(1)根據溶解度曲線知在40 ℃時,A、B兩物質的溶解度相等;(2)B的溶解度受溫度影響變化不大,可利用蒸發結晶法從溶液中得到B;(3)“冬天撈堿”說明堿的溶解度隨溫度的變化影響較大,故A的溶解度曲線與純堿相似。
答案:(1)40
(2)蒸發結晶
(3)A
22.(7分)下圖是一些常見物質的轉化關系,其中C是無色、無刺激性氣味的氣體,且能使澄清石灰水變渾濁;E是一種無污染的清潔能源,其燃燒產物是H。

請根據上圖回答下列有關問題:
(1)紅棕色粉末A和氣體C、E的化學式分別為:A![]() 、C 、E 。
、C 、E 。
(2)G轉化為H和A的反應類型是 反應;B轉化成E和D的反應類型是 反應。
(3)①A與鹽酸反應的化學方程式為 ;
②D與氯氣化合生成F的化學方程式為 。
解析:根據紅棕色粉末與CO在高溫條件下發生反應生成能使澄清石灰水變渾濁的氣體C,可推斷:A為Fe2O3,C為CO2,B為Fe;Fe與鹽酸反應生成的氣體E為H2,淺綠色溶液D為FeCl2,此反應為置換反應;FeCl2溶液中通入Cl2,生成黃色溶液F為FeCl3;FeCl3溶液中加入NaOH溶液生成紅褐色G沉淀為Fe(OH)3,由G到A和H的反應為2Fe(OH)3![]() Fe2O3+3H2O,該反應為分解反應。
Fe2O3+3H2O,該反應為分解反應。
答案:(1)Fe2O3 CO2 H2
(2)分解 置換
(![]() 3)①Fe2O3+6HCl
3)①Fe2O3+6HCl![]() 2FeCl3+3H2O ②2FeCl2+Cl2
2FeCl3+3H2O ②2FeCl2+Cl2![]() 2FeCl3
2FeCl3
四、實驗探究題(本題包括2個小題,共16分)
23.(6分)澄清石灰水是實驗室常用的試劑之一。如圖所示是同學們做過的實驗:
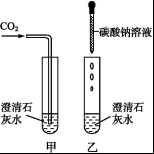
(1)甲中能觀察到的明顯現象是 ;![]()
(2)乙中的反應可用化學方程式表示為 。
解析:二氧化碳與氫氧化鈣反應生成白色沉淀碳酸鈣,故可以看到甲中的澄清石灰水變渾濁;碳酸鈉與氫氧化鈣反應生成碳酸鈣沉淀和氫氧化鈉。[來源:學科網]
答案:(1)澄清石灰水變渾濁(或產生白色沉淀)
(2)Ca(OH)2+Na2CO3![]() CaCO3↓+2NaOH
CaCO3↓+2NaOH
24.(10分)“家”是一個化學小世界,蘊含豐富的化學知識。
(1)分析下列與食品有關的化學物質,回答問題:
①某些食品中常加入防腐劑——苯甲酸(C6H5COOH)。該防腐劑屬于 (填“有機物”或“無機物”)。
②常用的食品干燥劑——生石灰(如圖),其干燥吸水的原理是 (用化學方程式表示)。分析圖中不可食用的原因是 (寫一點)。

③常用的食品脫氧劑——還原性鐵粉,其脫氧原理是:常溫下鐵與 和 共同作用而生銹。
(2)下表為幾種家用清潔劑的功能及有效成分:
名稱 | 潔廁靈 | 活氧彩漂 | 漂白精 |
功能 | 有效清除污垢與異味 | 漂洗使衣物色彩鮮艷[來源:學科網] | 快速漂洗衣物污漬 |
有效成分 | HCl | H2O2 | NaClO |
①不宜用“潔廁靈”清洗大理石地面的原因是 (用化學方程式表示)。欲測定“潔廁靈”的酸堿度,可選用 (填標號)。
A.pH試紙
B.酚酞溶液
C.石蕊溶液
②往“活氧彩漂”液體中加入少量二氧化錳,觀察到的現象是 ,反應的化學方程式為 。
③“潔廁靈”與“漂白精”不能混用,二者混合易產生一種有毒氣體X。其反應原理為:NaClO+2HCl![]() NaCl+X↑+H2O,則X的化學式為 。
NaCl+X↑+H2O,則X的化學式為 。
解析:(1)①含有碳元素的化合物是有機物,故苯甲酸屬于有機物;②氧化鈣能吸收水生成氫氧化鈣,故可做干燥劑,其反應的化學方程式為CaO+H2O![]() Ca(OH)2;因氧化鈣吸收水生成氫氧化鈣的過程中放出大量的熱,若食物中混入,則會灼傷食道;③由于鐵粉與氧氣、水反應生成鐵銹(氧化鐵),起到脫氧保鮮的作用;(2)①“潔廁靈”的有效成分為鹽酸,大理石的主要成分為碳酸鈣,而碳酸鈣與稀鹽酸反應生成氯化鈣、水和二氧化碳,該反應的化學方程式為CaCO3+2HCl
Ca(OH)2;因氧化鈣吸收水生成氫氧化鈣的過程中放出大量的熱,若食物中混入,則會灼傷食道;③由于鐵粉與氧氣、水反應生成鐵銹(氧化鐵),起到脫氧保鮮的作用;(2)①“潔廁靈”的有效成分為鹽酸,大理石的主要成分為碳酸鈣,而碳酸鈣與稀鹽酸反應生成氯化鈣、水和二氧化碳,該反應的化學方程式為CaCO3+2HCl![]() CaCl2+H2O+CO2↑;溶液的酸堿度一般用pH表示,常用pH試紙測定溶液的酸堿性,而紫色石蕊溶液、無色酚酞溶液只能測定溶液的酸堿性;②因為“活氧彩漂”主要成分為H2O2,故在盛有少量“活氧彩漂”的試管中,加少量二氧化錳,H2O2分解會有氧氣放出,觀察到的現象是有氣泡產生;其反應的化學方程式為2H2O2
CaCl2+H2O+CO2↑;溶液的酸堿度一般用pH表示,常用pH試紙測定溶液的酸堿性,而紫色石蕊溶液、無色酚酞溶液只能測定溶液的酸堿性;②因為“活氧彩漂”主要成分為H2O2,故在盛有少量“活氧彩漂”的試管中,加少量二氧化錳,H2O2分解會有氧氣放出,觀察到的現象是有氣泡產生;其反應的化學方程式為2H2O2![]() 2H2O+O2↑;③根據質量守恒定律可知,由NaClO+2HCl
2H2O+O2↑;③根據質量守恒定律可知,由NaClO+2HCl![]() NaCl+X↑+H2O可知,反應物中:Na原子為1個,Cl原子為3個,O原子為1個,H原子為2個;生成物中:Na原子為1個,Cl原子為1個,
NaCl+X↑+H2O可知,反應物中:Na原子為1個,Cl原子為3個,O原子為1個,H原子為2個;生成物中:Na原子為1個,Cl原子為1個,![]() O原子為1個,H原子為2個;還缺少兩個氯原子,故X是Cl2。
O原子為1個,H原子為2個;還缺少兩個氯原子,故X是Cl2。
答案:(1)①有機物 ②CaO+H2O![]() Ca(OH)2 生石灰遇水放出大量的熱會灼傷食道 ③氧氣 水
Ca(OH)2 生石灰遇水放出大量的熱會灼傷食道 ③氧氣 水
(2)①CaCO3+2HCl![]() CaCl2+H2O+CO2↑ A ②有氣泡冒出 2H2O2
CaCl2+H2O+CO2↑ A ②有氣泡冒出 2H2O2![]() 2H2O+O2↑ ③Cl2
2H2O+O2↑ ③Cl2
五、計算題(6分)
25.(6分)在實驗室里加熱30 g氯酸鉀(KClO3)和二氧化錳的混合物制取氧氣,完全反應后剩余固體質量為20.4 g。請計算:
(1)生成氧氣的質量為 g;
(2)原混合物中氯酸鉀的質量。
解析:解答本題的關鍵是利用質量守恒定律——化學反應前后物質的總質量不變,故反應后固體減少的質量即為生成氧氣的質量。根據氧氣的質量即可求出參加反應的氯酸鉀的質量。
答案:(1)9.6
(2)設混合物中氯酸鉀的質量為x。
2KClO3![]() 2KCl+3O2↑[來源:.Com]
2KCl+3O2↑[來源:.Com]
????????????? 245????????????? 96
????????????? x????????????? 9.6 g
245∶96=x∶9.6 g 解得x=24.5 g

孔乙己是貧困潦倒的知識分子。在書中,孔乙己是一個知識分子,滿口“之乎者也”,但是他很窮,還竊書,說過“讀書人的事,怎么能叫竊,”被人嘲笑,他...

自然界產生氧氣的化學方程式:光合作用的反應式為6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反應和暗反應兩個過程。需要具備光...

有的高校沒有條件,只要學業水平成績都合格就可以,比如中國科學院大學。有的需要平常學習考試成績,比如北京外國語大學要求高三第一學期期末成績在全...

在四則運算中,表示計算順序,在小括號之后、大括號之前;表示兩個整數的最小公倍數;表示取未知數的整數部分;在函數中,表示函數的閉區間;在線性代...

濟南開設的最好的職高學校有:濟南方信集團職業高中、濟南公共交通職業高中。濟南市公共交通職業高級中學是由濟南市公共交通總公司承辦,業務屬濟南市...

實然:是說事物實際上就是這樣的,但不同于現實性(現實性指其有合理性和客觀性);應然:就是應該是怎么樣的意思,比如說這件事,就應該是那樣的結果...

地中海氣候一種夏季炎熱干燥、冬季溫和多雨,雨熱不同期的氣候類型。地中海氣候冬季受西風帶控制,鋒面氣旋頻繁活動,氣候溫和,最冷月的氣溫在4-1...

堿石灰,又稱鈉石灰,堿石灰是白色或米黃色粉末,疏松多孔,是氧化鈣(CaO,大約75%),水(H?O,大約20%),氫氧化鈉(NaOH,大約3...